新版GMP 附录1:无 菌 药 品
第一章
范围
第一条 无菌药品是指法定药品标准中列有无菌检查项目的制剂和原料药,包 括注射剂、眼用制剂、无菌软膏剂、无菌混悬剂等。
第二条 本 附 录 适 用于 无 菌 制 剂 生 产全过 程 以 及 无 菌 原 料药的 灭 菌 和 无 菌 生 产过程。
第三条 悬浮粒子、浮游菌、沉降菌和表面微生物等测试方法应按照相关标准 执行。

第二章
原则
第四条 无菌药品的生产须满足其质量和预定用途的要求,应最大限度降低微 生物、各种 微粒和 热原 的污染。生 产人员 的技 能、所接受 的培训 及其 工作态度是 达到上述目 标的关 键因 素,无菌药 品的生 产必 须严格按照 精心设 计并 经验证的方 法及规程进 行,产 品的 无菌或其它 质量特 性绝 不能只依赖 于任何 形式 的最终处理 或成品检验。
第五条 无菌药品按生产工艺可分为两类:采用最终灭菌工艺的为最终灭菌产 品;部分或全部工序采用无菌生产工艺的为非最终灭菌产品。
第六条 无菌药品生产的人员、设备和物料应通过气锁间进入洁净区,如采用 机械连续传 输物料 时, 应采用正压 气流保 护并 监测压差。 物料准 备、 产品配制和 灌装或分装等操作必须在洁净区内分区(室)进行。
第七条 应按所需环境的特点确定无菌药品洁净生产区的级别。每一步生产操 作的环境都 应达到 适当 的动态洁净 度标准 ,以 尽可能降低 产品或 所处 理的物料被 微粒或微生物污染的风险。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
第三章
洁净度级别及监测
第八条 洁净区的设计必须符合相应的洁净度要求,包括达到“静态”和“动态” 的标准。
第九条 无菌药品生产所需的洁净区可分为以下 4 个级别:
A 级
高风险操作区 ,如: 灌装区、放 置胶 塞桶、 敞口安瓿瓶 、敞口西林 瓶的区域 及无菌装配或连接操作的区域。通常用层流操作台(罩)来维持该区的环境状态。 层流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s (指导值)。应有数据证 明层流的状态并须验证。
在密闭的隔离操作器或手套箱内,可使用单向流或较低的风速。
B 级
指无菌配制和灌装等高风险操作 A 级区所处的背景区域。
C 级和 D 级
指生产无菌药品过程中重要程度较低的洁净操作区。

以上各级别空气悬浮粒子的标准规定如下表:
洁净度级别 | 悬浮粒子最大允许数/立方米 | |||
洁净度级别 | 静态 | 动态 | ||
洁净度级别 | ≥0.5μm | ≥5μm | ≥0.5μm | ≥5μm |
A 级 | 3520 | 20 | 3520 | 20 |
B 级 | 3520 | 29 | 352000 | 2900 |
C 级 | 352000 | 2900 | 3520000 | 29000 |
D 级 | 3520000 | 29000 | 不作规定 | 不作规定 |
第九条 无菌药品生产所需的洁净区可分为以下 4 个级别:
A 级
高风险操作区 ,如: 灌装区、放 置胶 塞桶、 敞口安瓿瓶 、敞口西林 瓶的区域 及无菌装配或连接操作的区域。通常用层流操作台(罩)来维持该区的环境状态。 层流系统在其工作区域必须均匀送风,风速为0.36-0.54m/s (指导值)。应有数据证 明层流的状态并须验证。在密闭的隔离操作器或手套箱内,可使用单向流或较低的风速。
B 级
指无菌配制和灌装等高风险操作 A 级区所处的背景区域。
C 级和 D 级
指生产无菌药品过程中重要程度较低的洁净操作区。
以上各级别空气悬浮粒子的标准规定如下表:
洁净度级别 | 悬浮粒子最大允许数/立方米 | |||
洁净度级别 | 静态 | 动态 | ||
洁净度级别 | ≥0.5μm | ≥5μm | ≥0.5μm | ≥5μm |
A 级 | 3520 | 20 | 3520 | 20 |
B 级 | 3520 | 29 | 352000 | 2900 |
C 级 | 352000 | 2900 | 3520000 | 29000 |
D 级 | 3520000 | 29000 | 不作规定 | 不作规定 |
(1) 为了确定A级区的级别,每个采样点的采样量不得少于1m 。A级区空气尘 埃粒子的级别为ISO 4.8,以≥0.5μm的尘粒为限度标准。B级区(静态)的空气尘埃 粒子的级别为ISO 5,同时包括表中两种粒径的尘粒。对于C级区(静态和动态) 而言,空气尘埃粒子的级别分别为ISO 7和 ISO 8。对于D级区(静态)空气尘埃粒 子的级别为ISO 8。测试方法可参照ISO14644-1。(2) 在确认级别时,应使用采样管较短的便携式尘埃粒子计数器,以避免在远 程采样系统长的采样管中≥5.0μm 尘粒的沉降。在单向流系统中,应采用等动力学 的取样头。
(3) 可在常规操作、培养基模拟灌装过程中进行测试,证明达到了动态的级别, 但培养基模拟试验要求在“最差状况”下进行动态测试。
第十条 应对洁净区的悬浮粒子进行动态监测。
1. 根据洁净度级别和空调净化系统验证中获得的结果及风险评估,确定取样 点的位置并进行日常动态监控。
2. 在关键操作的全过程,包括设备组装、应对A级区进行微粒监测。工艺的 污染(如活 生物、 放射 危害)如可 能损坏 粒子 计数仪时, 应在设 备调 试操作和模 拟操作期间进行测试。A级区监测的频率及取样量,应能及时发现所有人为干预、 偶发事件及 任何系 统的 损坏。灌装 或分装 时, 由于产品本 身产生 粒子 或液滴,灌 装点≥5μm粒子也许不能始终如一地符合标准,这种状况是可以接受的。
3. 在B级区可采用相似于A级区的监测系统。根据B级区对相邻A级区的影响 程度,采样频率和采样量可予以调整。
4. 悬 浮 粒 子 的 监 测 系 统 应 考 虑 到 采 样 管 的 长 度 和 弯 管 的 半 径 对 测 试 结 果 的 影响。
5. 日 常 监 测 的 采 样 量 可 与 洁 净 度 级 别 和 空 调 净 化 系 统 验 证 时 的 空 气 采 样 量 不同。
6. 在A级区和B级区,连续或有规律地出现少量≥5.0 μm粒子计数时,可能是 污染事件的征兆,应进行调查。
7. 生产操作全部结束,操作人员撤离生产现场并经15~20分钟(指导值)自 净后,洁净区的悬浮粒子应达到表中的“静态”标准。
8. 对C级区和D级区应按照质量风险管理的原则进行动态监测。监控要求以及 警戒/纠偏限度可根据所从事操作的性质来确定,但自净时间应达到规定要求。
9. 温度、相对湿度等其它指标取决于产品及操作的性质,这些参数不应对规 定的洁净度造成不良影响。
第十一条 为 评 估无 菌生产 的微生物 状况, 应对微 生物进行 动 态监 测 ,监测 方法有沉降 菌法、 定量 空气浮游菌 采样法 和表 面取样法( 如:棉 签擦 拭法和接触 碟法)等。 动态取 样应 避免对洁净 区造成 不良 影响。成品 批记录 的审 核应同时考 虑环境监测的结果。
对表面和操作 人员的 监测,应在 关键 操作完 成后进行。 在正常的生 产操作监 测外,可在系统验证、清洁或消毒等操作完成后增加微生物监测。
中晶(嘉兴)半导体有限公司年产480万片12英寸硅片项目位于嘉兴 ...

ISO 16890是指根据ISO16890-1、ISO16890 ...

公告:中车时代电气(03898)拟将半导体业务的资产进行重组。 ...

空气过滤器的滤速与面风速计算公式衡量空气过滤器的通过风量的能力可 ...
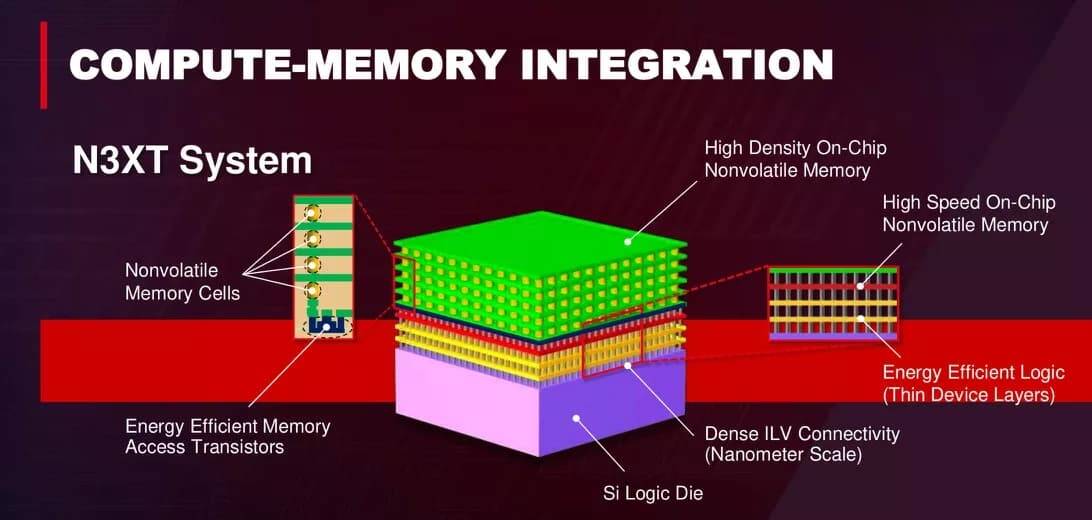
“毋庸置疑,摩尔定律依然有效且状况良好,它没有死掉、没有减缓、也 ...

纳米纤维过滤器材料研究团队证明,将纤维直径从200纳米减小到20 ...

珠海方正科技多层电路板有限公司(简称“珠海多层”,暂定为项目实施 ...

洁净层流罩是风机以一定的风速将经过预过滤后的空气 压入静压 ...

美国医疗器械制造商CytoSorbents Corp通过其血液过 ...

Clean Air Delivery Rate简称:CADR ...
因为GMP指南提供了预防交叉污染的建议,当实施风险评估时,可以合 ...

指南强调了领导参与和战略的重要性 有效的质量管理体系要求领导者 ...

作为研发和质量管理体系的重要一环,实验室管理,是确保研发及生产的 ...

香港在2003年公布了室内空气质量标准,在标准中对室内空气制订了 ...

无菌药品是指法定药品标准中列有无菌检查项目的制剂和原料药,包 括 ...

我国自主研发的首款商用“100G硅光收发芯片”正式投产使用。该系 ...
2017年7月6日,宁夏银和半导体科技有限公司承担的国家电子信息 ...

6.2.1 洁净室(区)与周围的空间必须维持一定的压差,并应按工 ...